- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Основное уравнение состояния
Выражения, связывающие значения любой из функций состояния со значениями координат состояния, есть однозначные уравнения состояния термодинамической системы: U = U(S, V, …), Т = T(S, V, …), р = p(S, V, …) и т.п.
Если для простой термомеханической системы из уравнения Т = T(S, V) выразить энтропию через температуру и объем S = S(T, V), то можем получить зависимость, связывающую между собой те параметры системы, которые могут быть измерены:
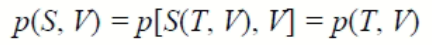
или
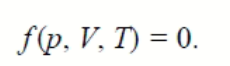
Состояние системы в таком случае определяется любой парой параметров, то есть любые два параметра из трех могут быть использованы в качестве независимых переменных.
При этих условиях свойства всех газов весьма схожи и их состояние описывается одинаковым для всех газов уравнением состояния идеального газа (уравнением Клапейрона‒Менделеева):
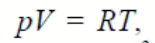
где V ‒ объем 1 кмоля вещества, м3/кмоль; R = 8,314 кДж/(кмоль·К) ‒ универсальная газовая постоянная, одинаковая для всех газов.
Уравнения состояния, предложенные для реальных газов, представляют собой, по существу, модификации уравнения состояния идеального газа, например уравнение Вандер-Ваальса:
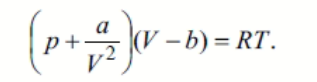
Или уравнение Камерлинг-Оннеса (1901). Оно выражает отклонение от уравнения состояния идеального газа в виде бесконечного степенного ряда по плотности:
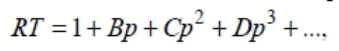
где В, С, D, … ‒ второй, третий, четвертый и т.д. коэффициенты, зависящие от температуры и природы газа и определяются экспериментально.
В химической термодинамике к газообразным веществам обычно применяют законы идеальных газов. Это упрощает расчеты и обеспечивает получение удовлетворительных результатов.
Поскольку изменение состояния сложной системы сопровождается изменением количества (массы) вещества в отдельных ее составляющих, то для полной характеристики состояния системы необходимо помимо термомеханических координат (S и V указывать также все химические координаты состояния.
Следовательно, уравнение состояния сложной системы связывает функцию состояния системы не только с двумя термомеханическими параметрами, определяющими состояние системы в процессе взаимодействия ее с окружающей средой, но и со значениями характеристики состава для всех составляющих сложной системы, определяющих состояние системы при фазовом или химическом взаимодействии между ее составляющими внутри системы, например:

n = vi – количество молей вещества в системе.
Статьи по теме
- Оценка возможных последствий взрыва для здания и персонала
- Неразрушаемые предохранительные конструкции производственных помещений
- Оценка возможности и целесообразности уменьшения площади разлива
- Оценка возможности снижения аварийной массы горючего вещества
- Оценка последствий детонационного взрыва для смежного объекта
- Оценка последствий взрыва в помещении
- Закон постоянства сумм тепла
- Воздух как окислитель во взрывоопасных воздушных смесях
- Основное уравнение процесса и энтальпия
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

