- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Термодинамические потенциалы системы
Для термодинамического описания процессов в закрытых системах кроме внутренней энергии и энтропии применяют еще несколько величин – функций состояния системы (табл. 1.1), значения которых определяются параметрами системы, а их изменение при протекании процесса можно рассчитать, пользуясь первым и вторым законами термодинамики.

Можно доказать, что в закрытых системах, не производящих никакой работы кроме работы расширения системы (механической работы), выполняются соотношения:
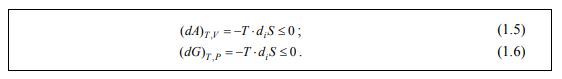
Соотношения (1.5), (1.6) – очень важны. Из них следует, что в согласии со вторым законом термодинамики (1.4) будут справедливы следующие утверждения.
При постоянном объеме и температуре всякая закрытая система всегда будет изменяться до тех пор, пока она не достигнет насколько возможно низкой энергии Гельмгольца.
Это может быть обусловлено снижением внутренней энергии или увеличением энтропии. При постоянном давлении и температуре всякая закрытая система будет изменяться до тех пор, пока она не достигнет самого низкого значения свободной энергии Гиббса.
Интересно
Итак, свободная энергия является свойством, определяющим возможность протекания процесса. Чаще всего, чтобы определять направление процесса в закрытых системах, приходится пользоваться свободной энергией Гиббса (G), так как температура и давление довольно просто контролируются в реальных условиях.
Изменение свободной энергии системы ( кон нач)(1)(2 ∆=− GGG ) в результате протекания термодинамического процесса можно рассчитать по уравнению (1.7).

Из уравнения видно, что величина ( ∆G ) складывается из двух составляющих: энтальпийного члена ( кон НН нач)(1)(2 ∆=− H ), величина которого связана с изменением энергии системы, и энтропийного ( ∆ST ), характеризующего изменение хаотичности системы
Основное уравнение для расчета изменения свободной энергии системы, находящейся при постоянных давлении и температуре, указано выше.
Часто по умолчанию допускается, что ∆Н и ∆S не зависят от температуры, и это действительно часто оказывается справедливым при условии небольшого температурного диапазона. Необходимо заметить, что влияние изменения энтропии при высокой температуре будет больше, чем при низкой.
Величины G и A имеют еще и дополнительный физико-химический смысл. Уменьшение свободной энергии Гельмгольца в каком-либо процессе, протекающем при T = const , V = const , равно максимальной работе, которую может совершить система в этом процессе.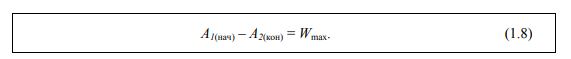
Таким образом, энергия Гельмгольца А равна той части внутренней энергии (U = А+TS), которая может превратиться в работу. Аналогично, уменьшение энергии Гиббса в каком-либо процессе при T = const , P = const равно максимальной полезной (т. е. немеханической) работе (Wmax ′ ), которую может совершить система в этом процессе (1.9):
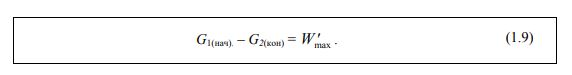
Максимальное количество электрической работы может быть получено за счет протекания токообразующей реакции в обратимых условиях и будет в точности равно убыли свободной энергии гальванического элемента. Если реакция идет необратимым путем, то произведенная электрическая работа Wэл будет меньше (1.10):
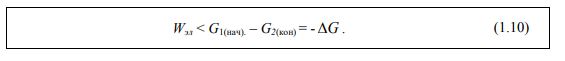
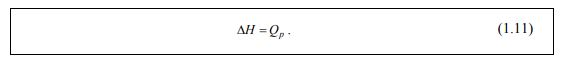
Поэтому изменение энтальпии ( ∆H ) может быть измерено калориметрическим путем как количество выделившегося в окружающую среду тепла. (Изменения энтропии, как правило, не могут быть измерены непосредственно.)
Статьи по теме
- Силы внутреннего трения жидкости. Уравнение Ньютона
- Идеальные модели деформирующихся систем
- Основные понятия реологии
- Учение о процессах деформации систем
- Теория абсолютных скоростей реакции
- Температурная зависимость скорости реакции
- Теория Дебая–Хюккеля
- Растворы электролитов при диссоциации
- Самоассоциация и электрическое экранирование
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

